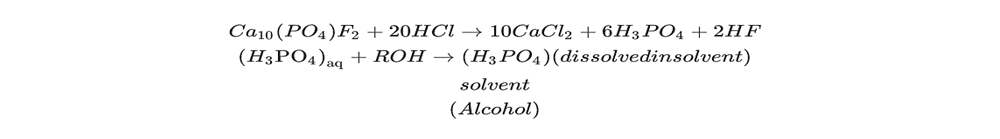GHS pictograms (GHS: International Globally Harmonized System of Classification and Labelling of Chemicals)
GHS signal word (Danger or Warning)

….(TWA) TWA: Time weighted average …(STEL) STEL: Short Term Exposure Limit
LD50 (median dose)
LC50 (median concentration)
LCLo (lowest published)
ثبت سفارش و صدور پیش فاکتور
راهنمای ثبت سفارشبا تشکر از شما ثبت سفارش با موفقیت انجام شد
برای پیگیری وضعیت سفارش و پرینت پیش فاکــــتور صـــادر شده لطفا کد رهــگیری فوق را یاداشت نمایید.
با استفاده از کد رهگیری می توانید:
- سفارش خود را کنسل کنید
- وضعیت سفارش خود بررسی نمایید.
- پیش فاکتور موقت و یا فاکتور نهایی آنلاین را دریافت نمایید.
توضیحات عمومی
|
خصوصیات فیزیکی شیمیایی فسفوريك اسيد |
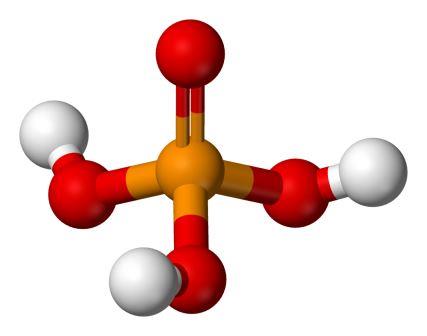
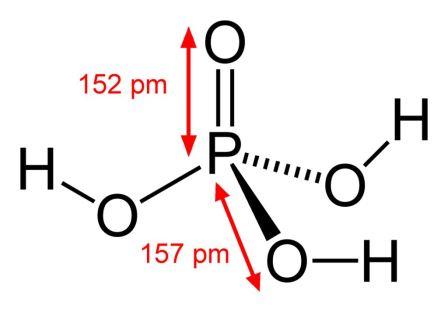
| رنگ، بو، حالت فیزیکی و خصوصیات فیزیکی معروف:
فسفوريك اسيد یک مایع شفاف، بی رنگ، بی بو و غیر فرار و یا جامد یک جامد کریستاله ی شفاف است که می تواند باعث خوردگی فلزات و سطح پارچه شود. در فرمولاسیون خود دارای یک اتم فسفر، سه اتم هیدروژن و چهار اتم اکسیژن است. فسفریک اسید یک عامل جداسازی[۱] است که برای جدا کردن کاتیون های ۲بار مثبت مانند Fe++ ، Mg++ ، Cu++ و Ca++ استفاده می شود. (pubchem) حلالیت در حلالهای دیگر و آب: انحلال پذیری در آب : ۱۰۰۰mg/ml انحلال پذیر در الکل ها مانند اتانول، اترها |
شرکتهای تولیدکننده فسفوريك اسيد |
| تولیدکنندگان ایرانی:
فسفوريك اسيد در حال حاضر توسط پتروشیمی رازی و ۵ شرکت خصوصی تولید می شود. |
| تولیدکنندگان خارجی:
آمریکا، چین، تایلند، ترکیه، برزیل، آفریقای جنوبی، سنگاپور و انگلستان |
ميزان واردات و صادرات فسفوريك اسيد (كد تعرفه گمركي . ۲۸۰۹۲۰۱۰) |
آمار واردات؛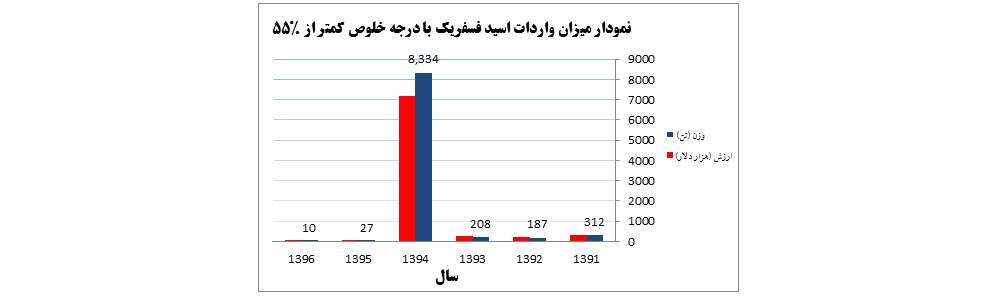
نمودار شماره یک – نمودار میزان واردات اسید فسفریک از سال ۱۳۹۶ – ۱۳۹۱ |
آمار صادرات؛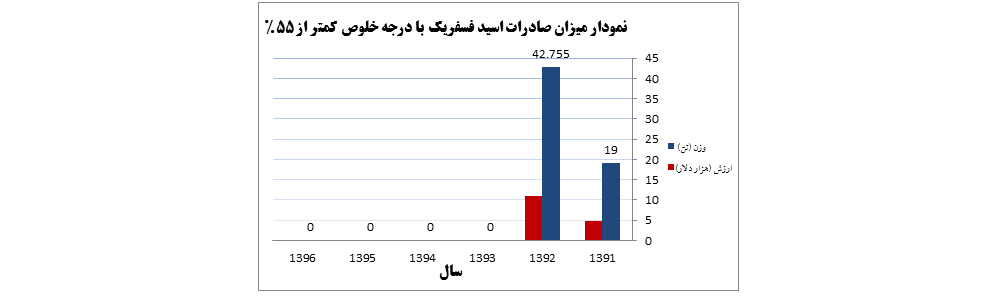
نمودار شماره دو – نمودار میزان صادرات اسید فسفریک از سال ۱۳۹۶ – ۱۳۹۱ |
کاربردهای فسفوريك اسيد |
||
صنایع مصرف کننده فسفوريك اسيد به ترتیب میزان مصرف:۱) صنعت چسب : چسب های اپوکسی که به منظور اتصال مستقیم تجهیزات ارتودنسی استفاده می شوند، حاوی اسید فسفریک هستند که در صد آن بر روی میزان مقاومت چسب تاثیر به سزایی دارد. (D.H. Retief, 1975) ۲) داروسازي و درمان : در دندانپزشکی در فرآیند اچ کردن[۲] از یک ژل اسیدی برای ایجاد سطح سخت میکروسکوپیک بر روی مینا یا عاج دندان به منظور ایجاد قابلیت پیوند با رزین استفاده می شود که این ژل ها حاوی فسفریک اسید بوده و این اسید به عنوان یک محلول اچینگ[۳] شناخته می شود. محلول های ایچینگ برای تمیز کردن سطح دندان استفاده می شوند. فسفوريك اسيد برای تمیز کردن دندان، تولید دهانشویه ها و داروهای ضد تهوع نیز مورد استفاده قرار می گیرد. ترکیب شدن اسید فسفریک با روی منجر به تولید فسفات روی می شود که از آن به عنوان یک ترکیب پرکننده ی دندان استفاده می شود. در جرم گیری دندان برای از بین بردن پلاک ها نیز از فسفوريك اسيد استفاده می شود. (Science Struck) (D.H. Retief, 1975) (دندال) (byjus) ۳) صنعت کشاورزی : به دلیل خورنده بودن فسفوريك اسيد به طور مستقیم به عنوان کود استفاده نشده و به صورت نمک های فسفات مانند سوپر فسفات سه گانه[۴]، دی آمونیوم هیدروفسفات[۵] و مونو آمونیوم دی هیدروژن فسفات[۶] مورد استفاده قرار می گیرد. حدود ۸۰% از اسید فسفریک تولیدی در تولید کود استفاده می شود. هم چنین از آن به عنوان یک طعم دهنده در خوراک دام و طیور استفاده می شود. (byjus) (Benjamín Valdez Salas, 2017) (essential chemical industry) ۴) صنعت متالوژی : در این صنعت برای تصفیه ی سطوح فلزات از فسفریک اسید استفاده می شود. (Benjamín Valdez Salas, 2017) ۵) صنایع غذایی : در صنایع غذایی جهت تنظیم اسیدیته ی برخی مواد خوراکی مانند مربا، گوشت های پردازش شده، غلات، پنیر و … و در تولید نوشیدنی ها از آن به عنوان یک اسیدولانت استفاده می شود. اسیدولانت ها ترکیباتی هستند که به مواد غذایی طعم ترش داده و از رشد باکتری ها و قارچ ها جلوگیری می کنند. (byjus) ۶) صنایع آرایشی – بهداشتی : به منظور تنظیم PH محصولات مراقبت شخصی مانند شوینده های مورد استفاده در حمام، محصولات مراقبت از ناخن، رنگ موها و محصولات مراقبت از پوست از فسفوريك اسيد استفاده می شود. (byjus) ۷) صنایع شیمیایی : از فسفوريك اسيد به عنوان یک الکترولیت در سلول های سوختی و ژنراتورهای اکسید هیدروژن استفاده می شود. هم چنین در تصفیه ی آب و فلزات نیز مورد استفاده است. از دیگر کاربردهای آن تولید فسفات های به کار رفته در مواد شوینده مانند تری سدیم فسفات و سدیم تری پلی فسفات است ولی استفاده از فسفوريك اسيد در شوینده ها و تمیز کننده های خانگی به دلیل احتمال آسیب به سیستم فاضلاب شهری متداول نمی باشد ولی در پاک کننده های صنعتی که پیش از انجام فرآیند اصلی برای آماده سازی سطوح استفاده می شوند ( مانند فرآیند آبکاری و رنگ کردن ) حاوی فسفوريك اسيد هستند. (finishing.com) (byjus) ۸) صنعت ساختمان : پاک کننده ها و تمیزکننده های مورد استفاده در صنعت ساختمان که برای از بین بردن لکه های سیمان، لکه های آب سخت و پسماندهای معدنی استفاده می شوند حاوی فسفوريك اسيد هستند. (Science Struck) ۹) صنعت الکترونیک : در تولید میکروساخت ها به منظور حکاکی بر روی سیلیکون نیتریدها از فسفریک اسید داغ استفاده می شود. فسفریک اسید غلیظ به عنوان فسفریک اسید گرید الکترونیکی شناخته می شود و در تولید نیمه هادی ها، پانل های صفحات نمایش و قرص های سیلیسیم[۷] برای تمیز کردن سطوح استفاده می شود. (Science Struck) (PERSISTENCE) ۱۰) صنعت قند : پس از برداشت چغندر قند و نیشکر، آن ها را با آب وارد واکنش کرده تا شیره خام که دارای PH پایین و ناخالصی های بسیار است، تولید شود. در مرحله ی بعد کلسیم هیدروکسید ( آهک ) جهت افزایش PH و واکنش با ناخالصی ها و تشکیل ترکیبات آلی کلسیم نامحلول به شیره ی خام افزوده می شود (Ca2++ + HPO– –۴→ CaHPO4). مقادیری اضافی آهک که وارد واکنش نشده اند، به وسیله ی فسفریک اسید جداسازی می شوند. جهت دست یابی به غلظت مطلوب این فرآیند چندین بار تکرار می شود. (Encyclopedia Britannica) (GRAYMONT) (Suger Process Technologies) ۱۱) صنعت نساجی : رنگ های اسیدی که به طور معمول برای رنگ آمیزی پروتئین های طبیعی ( پشم و ابریشم )، پلی آمید مصنوعی (نایلون) و فیبرهای آکریلیک استفاده می شوند، در حین فرآیند رنگرزی نیاز به یک ترکیب تنظیم کننده PH دارند که فسفریک اسید یکی از آن هاست. از مشتقات این اسید نیز برای تمیز کردن الیاف در صنعت نساجی استفاده می شود. (Sekar, 2011) |
||
فرايند توليد فسفوريك اسيد |
||
|
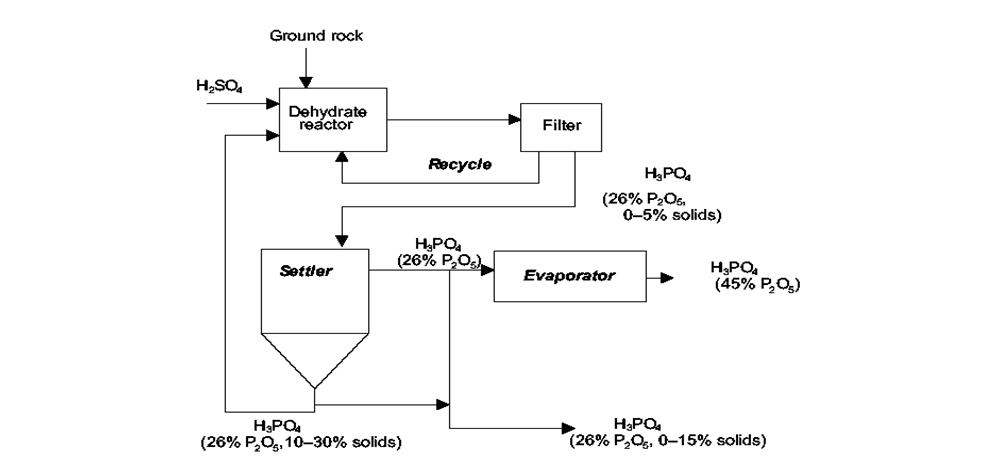
حجم تولید سالیانه فسفوريك اسيد در سالهای اخیر: این حلال در حال حاضر توسط ۵ شرکت خصوصی مجموعا به ظرفیت ۱۵۷۰۰۰تن تولید می شود. روشهای مختلف تولید فسفوريك اسيد:۱) روش تر ( wet processing ) : فسفوريك اسيد را می توان با تصفیه و حل کردن سنگ فسفات در اسیدهای معدنی مانند نیتریک اسید، هیدروکلریک اسید، سولفوریک اسید و یا فسفریک اسید به دست آورد. استفاده از سولفوریک اسید متداول تر بوده و با نام فرآیند مرطوب شناخته می شود. در این روش ابتدا سنگ فسفات خشک وخرد شده و سپس به طور پیوسته به همراه سولفوریک اسید وارد راکتور می شود. حاصل واکنش سولفوریک اسید و سنگ فسفات، سولفات کلسیم و اسید فسفریک است که پس از خروج از راکتور طی چند مرحله فیلتراسیون از یکدیگر جدا می شوند. بسته به شرایط عملیاتی کلسیم سولفات در دو فرم دی هیدارته[۸] و نیمه هیدراته[۹] می تواند تولید شود. در دمای C ˚ ۸۰-۷۰ کلسیم سولفات دی هیدراته و در دمای C ˚ ۱۱۰-۹۰ کلسیم سولفات نیمه هیدراته تولید می گردد. فرآیند دی هیدراته به دلیل سازگاری بیشتر با انواع سنگ ها و ساده تر بودن فرآیند محبوب تر بوده در حالی که فرآیند نیمه هیدراته منجر به تولید محصول با خلوص بیشتر می شودکه منجر به کاهش هزینه ها می گردد. به منظور افزایش خلوص اسید فسفریک از فرآیند تبخیر استفاده می شود. اسید تولید شده در این روش عمدتا برای تهیه ی کودها مورد استفاده قرار می گیرد. (Plant & Soil Sciences Library) (GUICHON) (Tariq F.Al-FarissH, 1992) Ca 10 F2 (PO4)6 + 14H3 PO4 ——-à ۱۰Ca (H2 PO4)2 +2HF ۱۰Ca (H2 PO4)2 + 10H2 SO4+20H2O ——-à ۲۰H3 PO4 + 10Ca SO4 . 2HO2 واکنش نهایی : Ca10 F2 (PO4)6 + 10 H2 SO4 + 20 H2O ——-à ۶ H3 PO4 + 10 Ca SO4 . 2 H2O + 2 HF ۲) اسیدی شدن با هیدروکلریک اسید : سنگ فسفات باهیدروکلریک اسید وارد واکنش می شود و فسفریک اسید حاصل می گردد. برای استخراج فسفریک اسید از یک حلال آلی مانند الکل های ۴ تا ۵ کربنه و یا تری بوتیل فسفات[۱۰] استفاده می شود. وجود کلسیم کلرید در جریان برای فرآیند استخراج ضروری است. فاز آلی تغلیظ شده به وسیله ی واکنش با آب جداسازی شده و برای خالص سازی بیشتر اسید فسفریک فرآیند تبخیر انجام می شود. از مزایای این روش سریع بودن تجزیه ی سنگ فسفات در هیدروکلریک اسید، تولید اسید با خلوص بالا و بازیابی بیشتر فسفر پنتااکسید از مقدار سنگ کمتر است. (Tariq F.Al-FarissH, 1992) ۳) فرآیند Davison clinker : در این فرآیند سنگ فسفات با اسید سولفوریک قوی وارد واکنش می شود. در مرحله ی بعد محصولات واکنش به منظور دست یابی به موادی مشابه با کلینکر[۱۱] حرارت داده می شوند. شست و شوی کلینکرها منجر به تولید فسفریک اسید غلیظ می شود. در این روش در مقایسه با فرآیند مرطوب، مراحل فیلتراسیون و تبخیر حذف شده اند. از معایب این روش دشوار بودن استخراج از کلینکرها با توجه به تخلخل کم آنهاست. ۴) روش حرارتی ( Thermal processing ) : در این روش ابتدا سنگ فسفات خشک و خرد شده و به همراه کک (کربن) و کوارتز در کوره الکتریکی قرار می گیرد و واکنش زیر انجام می شود : Ca20 3Ca 3(PO4)20 + 9SiO2 + 15C —–à CaF2 + 3/2 P4 + 15 CO + 9 Ca SiO3 در مرحله ی بعد فسفر در واکنش با هوا اکسید شده و پنتااکسید فسفر تولید می شود. فسفریک اسید حاصل واکنش فسفرپنتااکسید با آب است. P4 + 5O2 ——-> 2P2O5 P2O5 + 3 H2O ——-> 2H3PO4 خروجی این روش درصد خلوص بالایی داشته و در تولید مواد شیمیایی با کیفیت بالا مانند داروها، شوینده ها و مواد غذایی استفاده می شود ولی تولید آن از نظر اقتصادی بسیار هزینه بر بوده و مقرون به صرفه نیست. (GUICHON) |
|
|
فهرست واژگان
[۱]– sequestering agent : ترکیبی که بدون انجام واکنش شیمیایی، با تشکیل حلقه یون ها را از محلول جدا می کند. این ترکیبات عمدتا برای از بین بردن سختی آب استفاده می شوند.
[۲]– Etching
[۳]– etching solution
[۴]– triple superphosphate (TSP)
[۵]– diamonium hydrogenphosphate (DAP)
[۶]– monoammonium dihydrogenphosphate (MAP)
[۷]– Wafer (electronics) : قرص سیلیسیم یا قرص سیلیکون یک برش نازک از یک نیمهرسانا مانند بلورهای سیلیسیم است که در ساخت تراشههای الکترونیکی و دیگر ریزابزارها کاربرد دارد.
[۸]– dihydrate
[۹]– hemihydrate
[۱۰]– tributylphosphate (TBP)
[۱۱]– clinker : کلینکر در تولید سیمان پرتلند، دانههای حرارت دیدهای است، که معمولاً ۳-۲۵ میلیمتر(قطر) دارند و از حرارت دادن به سنگ آهک و آلومینیوم سیلیکات (خاک رس) در طی مرحله کوره سیمان بوجود میآیند.